Diagnóstico Laboratorial de Patologías Digestivas a Partir de la Necropsia
Las enfermedades digestivas continúan siendo un importante problema económico para la industria porcina de nuestro país. En los últimos 10 años se ha publicado y hablado especialmente de enfermedades respiratorias y sistémicas, siendo los procesos digestivos el “pariente pobre” de la patología porcina.
No obstante, el mayor porcentaje de problemas en granjas de alta sanidad, libres de la mayoría de patógenos, suelen ser alteraciones digestivas, y éstas también suponen un componente importante en lo que se llama complejos de enfermedad, donde es frecuente la concomitancia de procesos respiratorios y digestivos. Por otro lado, la interpretación lesional al realizar una necropsia no es tarea fácil, dado que los cambios post-mortem o un estado avanzado de autolisis pueden inducir a errores importantes en el establecimiento del diagnóstico anatomo-patológico, que luego se pueden traducir en tratamientos inadecuados y, por tanto, ineficaces. Finalmente, el aparato digestivo es por definición un sistema “contaminado”, y la interpretación del papel etiológico de un aislamiento microbiológico o de la detección de un determinado agente en el tracto digestivo estudiado también puede ser causa de confusión.
Por ello, el objetivo de esta revisión es presentar aspectos prácticos de interpretación lesional, toma de muestras para envío a un laboratorio de diagnóstico y de interpretación de resultados laboratoriales. Con ello se pretende:
Identificar hallazgos patológicos que puedan explicar la sintomatología observada en la granja
Identificar los patógenos o factores (trauma, toxinas, ambiente, etc.) que se conoce puedan ser la causa de las lesiones observadas
Realización de necropsia — Toma y envío de muestras
El papel del veterinario clínico ante un caso de enfermedad es fundamental de cara al establecimiento del diagnóstico y de un programa terapéutico o preventivo efectivo. Para estos efectos, se necesita conocer la historia clínica del caso de forma precisa, realizar un examen clínico exhaustivo de los animales enfermos, conocer los aspectos epidemiológicos del proceso patológico, realizar estudios post-mortem sistemáticos, ordenados y completos, y, en caso de que se crea conveniente, tomar las muestras apropiadas para la realización de analítica laboratorial. Esta revisión se centrará básicamente en los dos últimos puntos:
Estudios post-mortem
La necropsia es una herramienta fundamental para el establecimiento preliminar (o definitivo) del diagnóstico de un problema clínico. Ello implica que la selección del animal o animales para necropsiar es un punto clave para conseguir el diagnóstico adecuado. Este punto es aún más importante si la problemática clínica corresponde a patología digestiva, dado que el aparato digestivo es el que más rápidamente entra en autolisis una vez el animal ha muerto (Fig. 1 y 2). Las características ideales del cerdo a necropsiar en caso de patología digestiva serían:
vivo o muerto en las últimas una o dos horas (no autolítico)
representativo del cuadro clínico observado en granja
caso agudo de la problemática (menos de 72 horas desde el inicio del problema)
no medicado o mínimamente medicado
Por otro lado, en prácticamente todos los casos se recomienda necropsiar dos o más animales, ya que, con un solo animal, es fácil que éste no sea realmente un caso representativo del problema.
La realización de la necropsia debería ser en todos los casos sistemática, ordenada y completa, aunque aparentemente la problemática de origen digestivo parezca clara y evidente. Ello es debido a que la mayoría de enfermedades con las que se está luchando actualmente son de origen multifactorial, y es importante enfocar el diagnóstico desde un punto de vista global, no solamente asociado a un sistema o aparato.
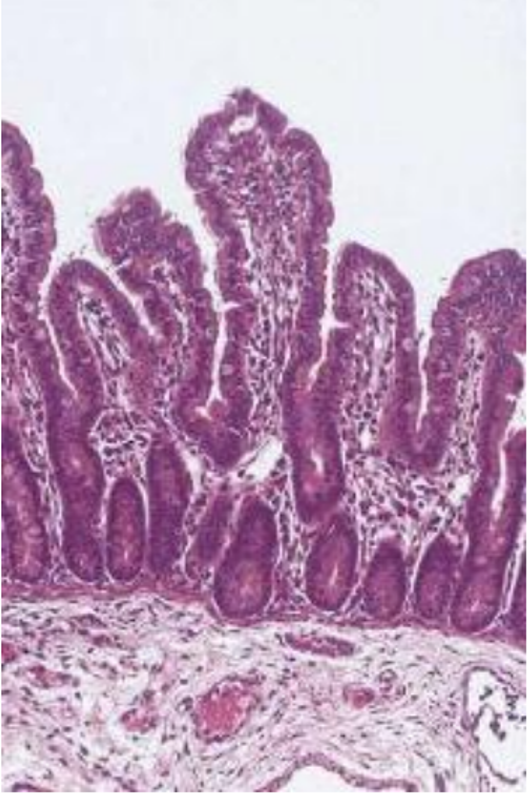
Fig. 1. Muestra de intestino delgado normal, correspondiente a un cerdo recién necropsiado y con una fijación inmediata de las muestras digestivas. Tinción de Hematoxilina y Eosina
Lógicamente, en caso de sospecha de alteración digestiva, se pondrá una mayor atención al tracto digestivo durante la necropsia. Teniendo en cuenta que el 99% de los problemas digestivos son de origen gastro-intestinal, en todos los casos sería estrictamente necesario el estudio del estómago (con apertura por la curvatura mayor) y la apertura de varias secciones intestinales, tanto de duodeno, yeyuno e ileon, como de ciego y colon. Tradicionalmente, por su localización en el interior de la cavidad pélvica, el recto es una zona poco estudiada, pero de importancia en algunas entidades patológicas.
El estudio macroscópico debe incluir (para ello es ideal contar con un cuchillo o bisturí, tijeras y pinzas para poder realizar la apertura de los distintos órganos):
Estómago:
Presencia o ausencia de contenido gástrico
Aspecto del contenido gástrico
Presencia de alteraciones de la mucosa gástrica:
Enrojecimiento [= congestión] (hallazgo normal y sin importancia patológica en la mayoría de casos; muy frecuente en caso de estómagos llenos de pienso; en caso de niveles elevados de uremia es frecuente una congestión intensa e incluso con leves hemorragias petequiales)
Manchas blanquecinas de diámetro variable, especialmente en animales lactantes y de transición (suelen asociarse a infecciones por Candida albicans)
Zonas necróticas de color verdoso oscuro o casi negro a ambos lados de la pars esofágica; generalmente se trata de micosis gástricas
Úlcera gástrica en pars esofágica de diámetro muy variable (corresponde al 99% de las lesiones macroscópicas gástricas); en los casos de úlceras gástricas muy crónicas, pueden llegar a cicatrizar y prácticamente ocluir el cardias (en esta situación, las capas musculares del esófago distal se encuentran hipertrofiadas)
Úlceras gástricas en regiones glandulares (muy raras en el cerdo; se pueden asociar al uso de antiinflamatorios no esteroidales vía oral o a la ingestión de substancias irritantes [en este caso suelen existir lesiones ulcerativas en el esófago])
Intestinos:
Coloración de la serosa (un color rojizo de la serosa NO es, necesariamente, equivalente a una lesión inflamatoria o enteritis)
Aspecto del contenido intestinal en las distintas secciones de intestino delgado y grueso. Se pueden considerar normales (en cerdos no lactantes) las siguientes situaciones:
Duodeno: contenido líquido verdoso o amarillento con presencia de partículas de pienso
Yeyuno: contenido líquido verdoso o amarillento, con o sin presencia de partículas de pienso; en algunos casos el contenido es líquido-pastoso
Ileon: contenido líquido verdoso, a veces líquido-pastoso, de color verde o amarillento
Ciego: contenido líquido o líquido-pastoso, de color verdoso
Colon: contenido pastoso a sólido, de color verde oscuro
Recto: heces formes de coloración oscura
Presencia de alteraciones de la mucosa intestinal (generalmente de origen inflamatorio: enteritis para designar una inflamación de yeyuno, duodenitis para el duodeno, ileitis para el ileon, tiflitis para el ciego, colitis para el colon y proctitis para el recto):
Ausencia de lesiones visibles con un contenido en intestino delgado más fluido del normal e incluso también fluido en intestino grueso (inflamación catarral); es la lesión inflamatoria más frecuente y se puede asociar a multitud de etiologías
Presencia de fibrina en el interior del tubo intestinal, especialmente del intestino delgado (inflamación fibrinosa); frecuente en casos de Salmonellosis
Presencia de fibrina adherida a la mucosa intestinal, con necrosis de ésta en las zonas con material fibrinoso (inflamación difteroide-necrotizante): frecuente en casos de Salmonellosis
Presencia de hemorragias en la mucosa (inflamación hemorrágica): la etiología dependerá de su localización
Presencia de abundante material mucinoso en la superficie del colon/recto, asociado a un contenido líquido o líquido-pastoso: frecuente en casos de infección por bacterias del género Brachyspira spp
Incremento del grosor de la pared del ileon, ciego y/o colon proximal: asociado especialmente a infecciones por Lawsonia intracellularis
En todos los casos es importante examinar otros órganos asociados al tracto gastro-intestinal. Por tanto, se recomienda también el estudio del hígado, páncreas, y linfonodos mesentérico y gastro-hepático.
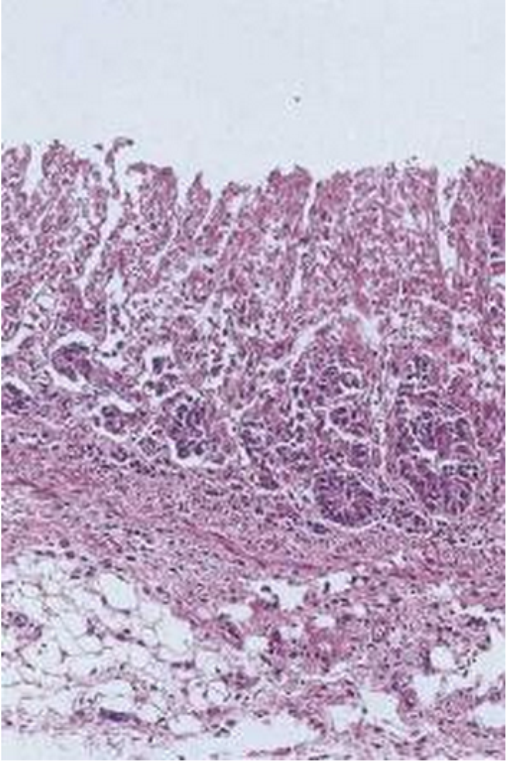
Fig. 2. Muestra de intestino delgado autolítico. Nótese la pérdida de estructura y la imposibilidad de identificar la estructura cripta-vellosidad. La autolisis empieza a ser un efecto evidente a las 2 horas post-mortem y complica / imposibilita el diagnóstico anatomo-patológico de las muestras estudiadas. Hematoxilina y Eosina.
Toma y envío de muestras
La fiabilidad del diagnóstico laboratorial no depende solamente de la sensibilidad y especificidad de las pruebas analíticas utilizadas, sino que la recepción de una muestra adecuada es el factor clave en la consecución del diagnóstico definitivo de un problema. Por ello, merece la pena resaltar la importancia crucial de la toma de muestras de cara a establecer el diagnóstico de una situación clínica. No obstante, la toma de muestras tiene varios componentes claves:
1. Elección de la muestra durante la realización de la necropsia
La toma de muestras se debe realizar durante la necropsia, no después de acabarla. Este hecho es tanto más importante cuando el tipo de analítica a realizar incluya el estudio microbiológico. Por definición, el aparato gastro-intestinal es un sistema “contaminado”. En general, se recomienda tomar las muestras de aparato digestivo después de haber tomado muestras (para estudio microbiológico) de otros órganos o tejidos que se quieran remitir a un laboratorio de diagnóstico, con la intención de no contaminarlos. Una vez realizada esta operación, se recomienda la selección de muestras para los estudios que se crean convenientes:
Estudio microbiológico:
Atar por los extremos las porciones intestinales seleccionadas y luego cortar por estos extremos; con esto se logra que no exista una sobre-contaminación del contenido intestinal anómalo que se pretende analizar. Utilizar contenedores estériles (es ideal un bote de plástico con cierre hermético). Alternativamente se pueden utilizar hisopos para la toma de muestras (se recomienda la utilización de hisopos con medio de cultivo en caso de que el laboratorio de diagnóstico reciba las muestras 12-24 horas después de ser tomadas)
Refrigerar la muestra de inmediato (es ideal la utilización de neveras portátiles cuando se realizan necropsias)
No congelar bajo ningún concepto (ello implica “matar” la mayoría de las bacterias que puedan ser la posible causa del problema digestivo; no sería un problema grave en caso de pretender solamente la dectección de virus por microscopia electrónica)
Estudio histopatológico:
Tomar muestras de intestino lo más pronto posible durante la realización de la necropsia
Tomar muestras de 5 a 10 cm de longitud y abiertas longitudinalmente por el borde mesentérico para facilitar el contacto de la mucosa con el formol al 10%
Utilizar contenedores de plástico con cierre hermético, llenados (4/5 partes de la capacidad) con formol al 10%
Mantener una proporción tejido:formol aproximadamente de 1:5-10, al menos (Fig. 3)
No necesita refrigeración para el envío al laboratorio correspondiente
La remisión de una muestra refrigerada para su posterior estudio histopatológico implica, normalmente, un transporte de al menos 12-24 horas. Ello implica que en el momento de fijar en formol en el laboratorio, la muestra se encontrará marcadamente autolítica (mínimamente útil para el estudio microscópico)
No congelar bajo ningún concepto (generación de artefactos que no permitirán un estudio microscópico adecuado)
Estudio parasitológico:
Tomar contenido intestinal en un bote de plástico de cierre hermético (estéril si es posible) de las zonas que se pretenden estudiar (dependerán del tipo de agente patógeno sospechado); idealmente, tomar muestras como en el estudio microbiológico, ya que la presencia de pared intestinal permite la realización de raspados de mucosa.
Refrigerar inmediatamente después de tomar la muestra
No congelar
Estudio toxicológico:
La muestra a tomar sería equivalente a la muestra tomada para el estudio microbiológico
Refrigerar o congelar para su envío al laboratorio
2. Referenciar el contenedor con la muestra
Es indispensable una correcta rotulación del contenedor de la muestra tomada, con identificación de granja, número de animal, y tipo de muestra que contiene. Este tipo de información debe incluirse también en la historia clínica que se remite al laboratorio de diagnóstico.
3. Empaquetar adecuadamente la muestra para su envío al laboratorio de diagnóstico
Este es otro punto clave en la estrategia de diagnóstico laboratorial. El paquete que se envía al laboratorio de diagnóstico debería incluir:
Un documento con la historia clínica de la granja y sospecha de la problemática. También debe incluir la técnica o técnicas que se solicitan al laboratorio de diagnóstico, teléfono y dirección de contacto del veterinario o persona que realiza el envío, y listado de las muestras remitidas
Las muestras correctamente etiquetadas y referenciadas en botes de plástico de cierre hermético (los botes de cristal se rompen con gran facilidad durante el transporte)
Sistema de refrigeración de muestras frescas para posibles estudios microbiológicos y parasitológicos
Referencia adecuada en el exterior del paquete a remitir, incluyendo claramente la dirección del remitente y la del laboratorio de destino Fig. 3. Tejidos fijados en formol. Se considera que el bote de la derecha permitirá una fijación adecuada dado que la proporción de formol es entre 5 y 10 veces mayor a la proporción de tejido. En el bote de la izquierda, el exceso de tejido imposibilitará una adecuada fijación y por tanto la autolisis de la muestra remitida.

4. Asegurar (en la medida de lo posible) un envío rápido de la muestra al laboratorio de diagnóstico
Tipo de muestras a remitir a un diagnóstico de laboratorio según patología sospechada
Este punto es una extensión del apartado sobre toma de muestras. Dependiendo de la causa sospechada, el tipo de muestra a remitir al laboratorio variará. En la tabla 1 se resumen las enfermedades digestivas más frecuentes del cerdo, la lesión más habitual que se les asocian, y el tipo de muestra a tomar en cada caso. No se incluye una referencia de la técnica laboratorial utilizada para detectar el agente o factor concreto que se pretende, dado que cada laboratorio utiliza un panel concreto de técnicas analíticas que, aunque permitan detectar el mismo agente o factor, pueden ser muy distintas. Para esta temática, en todos los casos, se recomienda que el veterinario clínico se ponga en contacto con el laboratorio que le ofrezca mayor confianza y que tome las muestras adecuadas para las técnicas que se utilicen en ese laboratorio concreto.
Analítica laboratorial
Existen una multitud de técnicas analíticas disponibles (según laboratorio) para la detección de agentes patógenos que pueden causar o estar involucrados en alteraciones digestivas en el cerdo. En este resumen no se incluyen las distintas técnicas laboratoriales existentes, dado que pueden ser muy variables para un mismo agente etiológico según laboratorio consultado. Lógicamente, las técnicas más utilizadas corresponden a aislamiento microbiológico (con antibiograma), detección de anticuerpos, histopatología, inmunohistoquímica (sobre tejido fijado en formol e incluido en parafina), inmunofluorescencia (sobre tejido congelado) y detección por PCR en heces.
Interpretación del resultado de la analítica laboratorial
En términos generales, los laboratorios de diagnóstico son marcadamente “microbiologistas”, ya que, básicamente, realizan determinaciones de agentes patógenos o anticuerpos frente a éstos. No obstante, el veterinario clínico que envía una muestra a un laboratorio de diagnóstico no puede ser simplista y aceptar sin más que el problema clínico con el que está luchando está causado por ese germen que le han detectado. El diagnóstico definitivo siempre será establecido por el veterinario responsable de la granja a través de: 1) historia clínica de la granja y características clínicas y epidemiológicas del problema actual, 2) datos obtenidos a través de la necropsia, y 3) resultados de la analítica laboratorial. Ello conlleva que la interpretación del resultado laboratorial tiene que ser consecuente con la situación clínica de la granja y de los datos patológicos obtenidos a la necropsia.
En algunos casos, el resultado laboratorial no satisface o explica la situación clínica ni las lesiones observadas. En estos casos, normalmente asociados a la detección de un agente concreto, se debe contemplar 1) que el microorganismo detectado no es la causa primaria del problema, aunque pueda estar involucrado en la problemática clínica de la granja, 2) que el microorganismo detectado si pueda ser la causa real del problema, de manera que habrá que reformular las hipótesis realizadas en la granja y ante la necropsia, o 3) que el microorganismo detectado indique una contaminación exógena no asociada a la problemática de la granja.
Tabla 1. Principales causas de inflamación intestinal en el ganado porcino, lesión macroscópica más frecuente que se le asocia y tipo de muestra a recolectar para el estudio laboratorial.
| ZONA ANATÓMICA | FASE DE PRODUCCIÓN | NOMBRE DE LA ENFERMEDAD | ETIOLOGíA | LESIÓN MÁS REPRESENTATIVA | MUESTRA/S A TOMAR |
| INTESTÍNO DELGADO | PARIDERA | Colibacilosis Coccidiosis Diarrea por Rotavirus Clostridiosis Gastroenteritis Transmisible (TGE) Diarrea Epidemica Vírica (DEV) Diarrea por Clostridium difficile | Escherichia coli Eimeria suis Rotavirus (grupo A) Clostridium perfringens (A y C) Virus de la TGE (Coronavirus) Virus de la DEV (Coronavirus) Clostridium difficile | Enteritis catarral Enteritis catarral a fibrino-necrótica Enteritis catarral (atrofia vellosidades*) Enteritis hemorrágico-necrotitzante Enteritis catarral (atrofia vellosidades*) Enteritis catarral (atrofia vellosidades*) Edema meso-cólico / Enteritis necrótica | Duodeno y/o yeyuno Yeyuno y/o ileon Yeyuno Yeyuno y/o ileon Yeyuno Yeyuno Yeyuno y colon |
| TRANSICIÓN / ENGORDE | Adenomatosis Intestinal Porcina Colibacilosis Salmonelosis Gastroenteritis Transmisible (TGE) Diarrea Epidemica Vírica (DEV) | Lawsonia intracellularis Escherichia coli Salmonella thyphimurium Virus de la TGE (Coronavirus) Virus de la DEV (Coronavirus) | Ileitis proliferativa y variantes Enteritis catarral a hemorrágica Enteritis catarral a fibrino-necròtica Enteritis catarral (atrofia vellosidades*) Enteritis catarral (atrofia vellosidades*) | Ileon Yeyuno y/o ileon Yeyuno y/o ileon Yeyuno Yeyuno | |
| ADULTOS | Adenomatosis Intestinal Porcina Salmonelosis | Lawsonia intracellularis Salmonella thyphimurium | Enteritis hipertrófica hemorrágica Enteritis catarral a fibrino-necròtica | Ileon Yeyuno y/o ileon | |
| INTESTINO GRUESO | PARIDERA | — | — | — | — |
| TRANSICIÓN / ENGORDE | Adenomatosis Intestinal Porcina Salmonelosis Disentería Porcina Espiroquetosis Intestinal Porcina Trichuriasis Colitis inespecífica | Lawsonia intracellularis Salmonella thyphimurium Brachyspira hyodysenteriae Brachyspira pilosicoli Trichuris suis Nutricional (?) | Ileitis proliferativa y variantes Enteritis catarral a fibrino-necròtica Colitis muco-hemorrágica Colitis muco-catarral Tiflocolitis muco-hemorrágica Enterocolitis catarral | Ciego y/o colon proximal Ciego y/ colon Colon medio y/o distal Colon medio y/o distal Ciego y/o colon proximal y medio Colon | |
| ADULTOS | Trichuriasis Oesophagostomiasis | Trichuris suis Oesophagostomum dentatum | Tiflocolitis muco-hemorrágica Tiflocolitis granulomatosa multifocal | Ciego y/o colon proximal y medio Colon |
* Lesión solamente visible microscópicamente (atrofia y fusión de vellosidades).
Fuente: Joaquim Segalés & Razas Porcinas.







